http://www.musculos.org/musculo-recto-interno.html
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
ESTOS ARTICULOS ESTAN RELCIONADOS CON ALUNAS PATOLIGIA OSEASY ARTICULARES
LA ARTROSCOPIA MONOARTRITIS PADIATRICA
Entrenamiento de fuerza en jóvenes: mitos y realidades.
http://www.cienciadeporte.com/congreso/04%20val/pdf/0entref.pd
Osteogénesis imperfecta con manifestaciones en el periodo neonatal
http://www.cienciadeporte.com/congreso/04%20val/pdf/0entref.pd
4ª) ETAPA DE PREPARACIÓN PARA LA COMPETICIÓN. Esta etapa
suele tener una duración entre 4 a 6 semanas y consiste en llegar a
trasladar todo lo entrenado en la etapa anterior a 1RM y por tanto hacer
la mejor marca conseguida hasta ese momento.
Como se comprenderá con este sistema de entrenamiento y alternándolo con los
descansos necesarios es muy difícil que el atleta joven tenga alguna lesión. Solo podría
ser en las competiciones ya que es donde se llegaría a 1RM. Somos conscientes que las
posibilidades de lesión aparecen cuando incrementamos la intensidad, para ello hemos
adoptado la formula de Berger para conocer 1RM sin haberla hecho, o sea un máximo
virtual.
Dicha formula ha sido modificada por nosotros al comprender que no contempla el
grado de cansancio de las series precedentes al test, por ello se le ha añadido un
coeficiente resultante de en qué serie se hace el citado test.
Vamos a aclarar esta cuestión:
La formula de Berger es: 1RM = K x R x 0,03 + K como valor aproximativo es válida
pero queriendo afinar mas hemos introducido los valores del número de repeticiones
máximas por porcentaje de distintos autores y corresponden todos ellos a una curva
cuya ecuación es:
y = 0,99913 – 110,19x + 3,9117e + 4x^2 – 2,8977e + 6x^3 + 7,7363e + 7x^4
Con esta curva encontramos los valores cambiantes del 0,03 que plantea Berger en
función de las repeticiones realizadas. 6
Resolviendo la ecuación nos salen los valores de 0,03 cambiantes con los siguientes
resultados:
Para 1 repetición el 0,03 = 0
Para 2 repetición el 0,03 = 0,013
Para 3 repetición el 0,03 = 0,018
Para 4 repetición el 0,03 = 0,020
Para 5 repetición el 0,03 = 0,022
Para 6 repetición el 0,03 = 0,023
Para 7 repetición el 0,03 = 0,024
Para 8 repetición el 0,03 = 0,025
Para 9 repetición el 0,03 = 0,026
Para 10 repetición el 0,03 = 0,027
A estos valores de la constante 0,03 le añadimos % de la serie en que se realizó el test.
Quedando la formula como sigue:
1RM = K x R x @ + K + %S
Siendo: K = los kilogramos realizados durante la serie del test.
R = las repeticiones máximas realizadas en dicha serie tets
@ = valor que toma 0,03 según las repeticiones realizadas.
%S = % a incrementar de K en función de en que serie se realiza el test.
Si a todas estas precauciones le añadimos que también hemos realizamos un estudio de
los 10 mejores levantadotes del mundo que consiguieron militar en la categoría de mas
de 105 Kg de peso corporal y ser reconocidos a nivel popular ( Kurlovich, Tarañenko,
Pisarenko, Rajmanov, Marchuk, Didyk, Akoev, Zajarevich, Sypko y Seroguin),
concluiremos diciendo que muchas de nuestras investigaciones han servido para aclarar
esos mitos que la población repite sin un conocimiento científico adecuado.
Para conocer el crecimiento y desarrollo de dichos levantadotes, hemos estudiado los
siguientes datos: Peso corporal, Estatura del atleta, Relación peso / talla,(Índice de
Ketle, Marcas de Arrancada, Dos Tiempos, Relación A / DT o arrancada partido
por dos tiempos y Total Olímpico.
Para representarlos gráficamente hemos realizado la media de cada uno de los datos
según edades.
El intervalo de edades estudiadas han sido aquellas en las que está presente con mayor
énfasis el crecimiento, de 16 a 20 años.
Todos a los 20 años eran de categoría Elite. 7
La media del peso corporal de cada edad ha ido incrementándose de forma exponencial,
igualmente la talla.
Si superponemos el peso y la talla vemos que el peso ha sido el de mayor incremento
debido a la hipertrofia que han conseguido estos atletas. 8
Con estos datos podemos concluir que: la Halterofilia no incide negativamente en el
crecimiento y desarrollo, si no todo lo contrario.
También observamos que el índice de Ketle se va incrementando con la edad o años de
entrenamiento y conserva la misma imagen que el resto de gráficas, hay un acelerón en
los primeros años tendiendo a buscar la horizontal en la etapa Élite.
http://www.scielo.sa.cr/scielo.php?pid=S0001-60022009000200011&script=sci_arttext&tlng=pt
Acta Médica Costarricense
versión impresa ISSN 0001-6002
Acta méd. costarric v.51 n.2 San José abr.-jun. 2009
CASOS CLÍNICOS
Osteogénesis imperfecta con manifestaciones en el periodo neonatal
(Neonatal Presentation of Osteogenesis Imperfecta)
Resumen:
Se reporta un caso de un paciente masculino de un día de vida extrauterina; producto de una madre de 20 años, primigesta, prima segunda de su pareja. Nace por cesárea por presentación pélvica, con líquido amniótico meconizado, con un peso al nacer de 2275 gramos (RNTPEG). Al examen físico el niño se encontraba flácido, con cianosis leve, fontanelas amplias con comunicación de la anterior con la posterior, ausencia de escama occipital, escleras azules, retrognatia, extremidades cortas y con crepitación al movimiento. En las radiografías óseas con fracturas múltiples, formación de callo óseo y cambios displásicos en metáfisis. Se diagnostica por parte de los genetistas una osteogénesis imperfecta (OI) y se da consejo genético a los padres. La OI es un conjunto de trastornos genéticos que afectan la integridad del tejido conectivo, debido a que se presentan mutaciones en la síntesis del colágeno, ya sean autosómicas dominantes o recesivas. En vista de que el diagnóstico es predominante-mente clínico y radiológico, se debe profundizar en los patrones óseos, ya que los pacientes pueden desarrollar cambios quísticos, densos o frágiles. A partir de este caso de OI tipo 2 severa se pretende discutir las diferencias entre los diferentes grupos.
Descriptores: osteogénesis imperfecta, neonatos, protocolágeno tipo I.
Abstract:
We report the case of a male patient with one day of life, his mother is a 20-yr-old gravida 1 para 1 male, there is parental consanguinity (second cousin). This patient born alive by Caesarean section in breech presentation with meconium stained amniotic fluid and birthweight 2275 g (small for gestational age term infant). Physical examination findings in this case are hypotonia, mild cyanosis, large anterior fontanelle, absence of occipital scale, blue sclera, retrognathia and shortening of the long bones whit crepitation. The radiografphic findings show numerous fractures, hyperplastic callus formation and dysplastic changes in metaphyses. He was diagnosed by the geneticists with OI and given genetic counseling to parents. The osteogenesis imperfecta has a genetic background that affects connective tissue integrity, associated with collagen synthesis mutations, being dominant or recessive autosomic inheritance. In the majority of cases, diagnosis of IO is easy on the basis of clinical and radiological findings; for this reason must be important to emphasize on bone structure studies, because patients may develop cystic, dense or fragile changes. This case presents a patient who has osteogenesis imperfecta type II; we pretend to discuss the differences between Ol’s types.
Key words: osteogenesis imperfecta, neonates, type I protocollagen.
Caso clínico
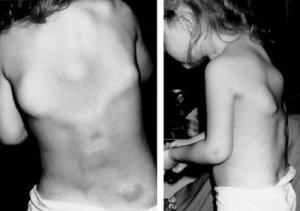
Se trata de un paciente masculino de un día de vida extrauterina, vecino de Corralillo de Cartago; producto de una madre de 20 años, primigesta (G1P1C1AO), quien acudió al control prenatal en ausencia de patologías durante el embarazo. El parto fue quirúrgico por medio de cesárea el 16 de julio de 2007, en el Hospital Max Peralta de Cartago; el niño se encontraba en presentación pélvica a las 38 semanas de edad gestacional; se describe que el líquido amniótico fue meconizado. El niño tuvo un peso al nacer de 2275 gramos, con una talla de 40 cm (pequeño para edad gestacional en peso y talla) y circunferencia cefálica de 33 cm; además, se catalogó con una puntuación de APGAR de seis al primer minuto, ocho a los cinco minutos y diez a los diez minutos. Se describe que al nacer el niño se encontraba flácido con cianosis leve y extremidades cortas. Le envían una radiografía de tórax que evidencia el parénquima pulmonar sin alteraciones, y fracturas en la clavícula izquierda, séptimo arco costal y húmero izquierdo; por estos hallazgos es trasladado al Hospital Nacional de Niños Dr. Carlos Sáenz Herrera con diagnóstico presuntivo de acondroplasia. Los hallazgos del examen físico al ingreso mostraron un paciente alerta, consciente, activo, eupneico, hidratado, con presión arterial de 71/52 mmHg, frecuencia cardíaca de 166 latidos por minuto, frecuencia respiratoria de 42 respiraciones por minuto y temperatura de 36.6°C. Se describen las fontanelas amplias con comunicación de la anterior con la posterior, ausencia de escama occipital, escleras azules, pupilas isocóricas normoreactivas, con movimientos extraoculares adecuados y retrognatia. La exploración cardiopulmorar no sugería alteraciones llamativas; con adecuada expansión torácica, únicamente presentaba dolor a la palpación de la parrilla costal bilateral. El abdomen tenía peristalsis, se notaba globoso, timpánico, sin visceromegalias, pero con separación de músculos rectos abdominales. Tenía genitales masculinos normales con testículos en escroto y ano permeable. En ese momento llamaba mucho la atención que ambas extremidades superiores eran cortas, con crepitación ósea, con leve deformidad en el miembro superior izquierdo, descrita como dorsiflexión de la muñeca con limitación de la extensión, inadecuada pronosupinación del antebrazo y, en general, poca movilidad de la mano izquierda (Figura 1). Las extremidades inferiores se describen cortas con leve deformidad en genuvaro; presentan edema, adecuada movilidad espontánea y tono, predominantemente en flexión.
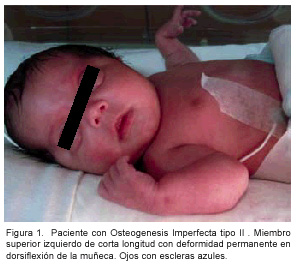
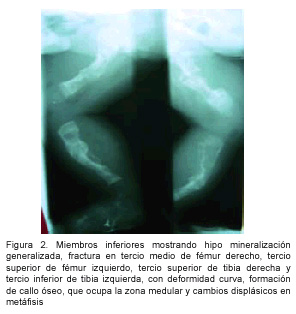
Los resultados de las pruebas de laboratorio al ingreso mostraron un hemograma sin datos patológicos. Fue valorado por el servicio de Ortopedia, que describe las radiografías de miembros inferiores mostrando hipomineralización generalizada, además, fractura en tercio medio de fémur derecho, tercio superior de fémur izquierdo, tercio superior de tibia derecha y tercio inferior de tibia izquierda, con deformidad curva, formación de callo óseo que ocupa la zona medular y cambios displásicos en metáfisis (Figura 2). A la vez se visualiza fractura de tercio medio de clavícula derecha y séptimo arco costal derecho, en el tercio medio con formación de callo óseo.
Patología articular
Patología articular inflamatoria del anciano en Atención Primaria
I. Moreno Gallego, A. Montaño Alonso*
Especialista en Reumatología. Sección de Reumatología. Hospital Universitario Virgen del Rocío.
*Especialista en Medicina Familiar y Comunitaria Centro de Salud Torreblanca. Sevilla
RESUMEN
Las enfermedades musculoesqueléticas agudas y crónicas afectan a individuos de todas las edades. El proceso de maduración y envejecimiento puede ser esquemáticamente dividido en cuatro periodos. La prevalencia de las enfermedades aumenta con la edad, a menos que estén asociadas con un aumento de la mortalidad como en el caso de la artritis reumatoide y de las enfermedades reumáticas sistémicas. Algunos ejemplos de enfermedades con diferencias en la incidencia y/o la expresión relacionadas con la edad incluyen artritis reumatoide, polimialgia reumática, arteritis de células gigantes, lupus eritematoso sistémico, artropatías microcristalinas y espodiloartropatías. En general, los mismos fármacos se usan en el tratamiento de las enfermedades reumáticas a todas las edades. El peso corporal y las diferencias metabólicas deben ser naturalmente consideradas y las dosis ajustadas para los diferentes grupos de edad.
Palabras clave: Envejecimiento. Enfermedades reumáticas inflamatorias. Atención Primaria.
Las enfermedades musculoesqueléticas agudas y crónicas afectan a individuos de todas las edades. El proceso de maduración y envejecimiento puede ser esquemáticamente dividido en cuatro periodos. La prevalencia de las enfermedades aumenta con la edad, a menos que estén asociadas con un aumento de la mortalidad como en el caso de la artritis reumatoide y de las enfermedades reumáticas sistémicas. Algunos ejemplos de enfermedades con diferencias en la incidencia y/o la expresión relacionadas con la edad incluyen artritis reumatoide, polimialgia reumática, arteritis de células gigantes, lupus eritematoso sistémico, artropatías microcristalinas y espodiloartropatías. En general, los mismos fármacos se usan en el tratamiento de las enfermedades reumáticas a todas las edades. El peso corporal y las diferencias metabólicas deben ser naturalmente consideradas y las dosis ajustadas para los diferentes grupos de edad.
Palabras clave: Envejecimiento. Enfermedades reumáticas inflamatorias. Atención Primaria.
Elderly inflammatory rheumatic disease in Primary Health Care
ABSTRACT
Acute and chronic musculoskeletal disorders affect individuals of all ages. The process of maturing and aging can be schematically divided into 4 periods. The prevalence of chronic disorders will increase with age, unless they are associated with an increasing mortality such as reumathoid arthritis and systemic rheumatic disorders. Some examples of disorders with age-related differences in incidence and/or expression include rheumatoid arthritis, polymyalgia rheumatica, giant cell arteritis, systemic lupus erythematosus, crystal artropathies and spondyloartropathies. In general, the same drugs are used in the treatment of rheumatic disease at all ages. Body weight and metabolic differences must naturally be considered and the dosage adjusted for different age groups.
Key words: Aging. Inflammatory rheumatic diseases. Primary Health Care.
Acute and chronic musculoskeletal disorders affect individuals of all ages. The process of maturing and aging can be schematically divided into 4 periods. The prevalence of chronic disorders will increase with age, unless they are associated with an increasing mortality such as reumathoid arthritis and systemic rheumatic disorders. Some examples of disorders with age-related differences in incidence and/or expression include rheumatoid arthritis, polymyalgia rheumatica, giant cell arteritis, systemic lupus erythematosus, crystal artropathies and spondyloartropathies. In general, the same drugs are used in the treatment of rheumatic disease at all ages. Body weight and metabolic differences must naturally be considered and the dosage adjusted for different age groups.
Key words: Aging. Inflammatory rheumatic diseases. Primary Health Care.
Aceptación: 06-11-01
INTRODUCCIÓN
Las enfermedades musculoesqueléticas agudas y crónicas afectan a individuos de todas las edades. La incidencia de estas enfermedades varía entre los grupos de edad, así como el dignóstico y tratamiento puede ser diferente en los distintos grupos de edad1.
El proceso de maduración y envejecimiento puede ser esquemáticamente dividido en 4 periodos. El primero es un periodo de crecimiento y maduración, seguido por una fase relativamente estacionaria; posteriormente sigue una fase de disminución gradual de la función, y finalmente una rápida fase terminal. Esta curva de envejecimiento varía entre órganos y tejidos y además la curva es diferente en cada individuo y, lo que es más importante, la variación aumenta con la edad2.
Esta variación tiene importantes consecuencias clínicas en la vejez que conducen a infradiagnosticar o a sobrediagnosticar enfermedades. En el primer caso puede ocurrir cuando la disminución de la función de un órgano se considera una reducción normal debida a la edad. En el segundo caso puede ocurrir porque los valores normales de la función de un órgano se basan frecuentemente en población joven; así, la presencia de una función reducida en un anciano puede ser incorrectamente considerada como signo de enfermedad3.
EDAD Y ENFERMEDADES REUMÁTICAS
La prevalencia de las enfermedades aumenta con la edad, a menos que estén asociadas con un aumento de la mortalidad como en el caso de la artritis reumatoide (AR) y de las enfermedades reumáticas sistémicas4. La incidencia de algunas enfermedades musculoesqueléticas aumenta con la edad y algunas sólo ocurren en pacientes mayores, por ejemplo polimialgia reumática, osteoporosis, artrosis y las enfermedades microcristalinas5.
Ciertos hallazgos específicos de enfermedades reumáticas asociados con diferentes grupos de edad se reconocen mejor en niños que en ancianos. Manifestaciones tardías de la enfermedad, como las complicaciones de algunas enfermedades inflamatorias crónicas, son relativamente frecuentes en el anciano, por ejemplo la amiloidosis, las vasculitis y el síndrome de Sjögren6. El comienzo de las enfermedades inflamatorias reumáticas puede variar en el anciano, por ejemplo en la AR y en el lupus eritematoso sistémico (LES), pero se le ha prestado poca atención en la práctica clínica. Además es muy frecuente la existencia de enfermedades concomitantes, lo que puede hacer el diagnóstico y el tratamiento más complicado que en el joven. Algunos ejemplos de enfermedades con diferencias relacionadas con la edad en la incidencia y/o expresión se muestran en la tabla I.
Las enfermedades musculoesqueléticas agudas y crónicas afectan a individuos de todas las edades. La incidencia de estas enfermedades varía entre los grupos de edad, así como el dignóstico y tratamiento puede ser diferente en los distintos grupos de edad1.
El proceso de maduración y envejecimiento puede ser esquemáticamente dividido en 4 periodos. El primero es un periodo de crecimiento y maduración, seguido por una fase relativamente estacionaria; posteriormente sigue una fase de disminución gradual de la función, y finalmente una rápida fase terminal. Esta curva de envejecimiento varía entre órganos y tejidos y además la curva es diferente en cada individuo y, lo que es más importante, la variación aumenta con la edad2.
Esta variación tiene importantes consecuencias clínicas en la vejez que conducen a infradiagnosticar o a sobrediagnosticar enfermedades. En el primer caso puede ocurrir cuando la disminución de la función de un órgano se considera una reducción normal debida a la edad. En el segundo caso puede ocurrir porque los valores normales de la función de un órgano se basan frecuentemente en población joven; así, la presencia de una función reducida en un anciano puede ser incorrectamente considerada como signo de enfermedad3.
EDAD Y ENFERMEDADES REUMÁTICAS
La prevalencia de las enfermedades aumenta con la edad, a menos que estén asociadas con un aumento de la mortalidad como en el caso de la artritis reumatoide (AR) y de las enfermedades reumáticas sistémicas4. La incidencia de algunas enfermedades musculoesqueléticas aumenta con la edad y algunas sólo ocurren en pacientes mayores, por ejemplo polimialgia reumática, osteoporosis, artrosis y las enfermedades microcristalinas5.
Ciertos hallazgos específicos de enfermedades reumáticas asociados con diferentes grupos de edad se reconocen mejor en niños que en ancianos. Manifestaciones tardías de la enfermedad, como las complicaciones de algunas enfermedades inflamatorias crónicas, son relativamente frecuentes en el anciano, por ejemplo la amiloidosis, las vasculitis y el síndrome de Sjögren6. El comienzo de las enfermedades inflamatorias reumáticas puede variar en el anciano, por ejemplo en la AR y en el lupus eritematoso sistémico (LES), pero se le ha prestado poca atención en la práctica clínica. Además es muy frecuente la existencia de enfermedades concomitantes, lo que puede hacer el diagnóstico y el tratamiento más complicado que en el joven. Algunos ejemplos de enfermedades con diferencias relacionadas con la edad en la incidencia y/o expresión se muestran en la tabla I.
PROBLEMAS ESPECIALES Y PRESENTACIONES EN EL ANCIANO
Los problemas musculoesqueléticos en los pacientes ancianos presentan un reto especial para el médico de Atención Primaria. Las quejas a menudo son vagas y mal definidas, multifactoriales, alteradas por condiciones coexistentes no relacionadas con el sistema musculoesquelético, y ocurren también con una disminución insidiosa de todas las funciones. Las pruebas de laboratorio y de imagen pueden ser mal diagnosticadas, debido a la frecuencia de hallazgos "anormales" en el anciano7. También la epidemiología y la historia natural de las quejas reumáticas son diferentes de las de los pacientes jóvenes8.
La evaluación funcional es fundamental para el estudio de un anciano con quejas musculoesqueléticas. La habilidad para levantarse de una silla, andar distancias cortas y asearse es la diferencia entre la vida independiente y requerir asistencia física o ingreso en una institución9.
ARTRITIS REUMATOIDE
La AR es una enfermedad poliarticular crónica caracterizada por una inflamación de las articulaciones con tendencia a la simetría, acompañada a veces de manifestaciones sistémicas extraarticulares10. Los progresos en el tratamiento en las últimas décadas han tenido como consecuencia una mejoría tanto del pronóstico funcional como del pronóstico vital de los enfermos, por lo que el número de pacientes que alcanza la edad geriátrica se ha incrementado11.
Estos pacientes deben ser diferenciados de aquéllos en los que el inicio de la enfermedad se produce a una edad avanzada, y que se denomina AR del anciano o de comienzo senil12.
De forma arbitraria se considera dentro de este concepto a los pacientes que inician la sintomatología después de los 60 años. La razón de la distinción entre AR del adulto y AR geriátrica es que la edad de presentación influye en el desarrollo de la enfermedad, apreciándose, al comparar ambos grupos de edad, características peculiares de la enfermedad en los ancianos respecto a la que se desarrolla a edades más tempranas13.
El diagnóstico de AR en el anciano puede ser difícil debido a su forma de presentación atípica, la presencia concomitante de artrosis, y la dificultad de distinguirla de la polimialgia reumática (PMR)14.
La AR clásica, con afectación sistémica de las articulaciones de las manos, muñecas, pies, y tobillos, con factor reumatoide positivo, predominio femenino y con un curso progresivo y destructivo se puede ver en ancianos como en jóvenes15. Sin embargo, un 25-40% de individuos que desarrollan artritis después de los 60 años tienen "AR be-nigna de la edad". Estos pacientes, a menudo hombres, presentan un comienzo abrupto de la enfermedad, afectación predominante de grandes articulaciones proximales (hombros, caderas y rodillas), factor reumatoide negativo, y frecuentemente presentan remisión espontánea en un año16. Existe un síndrome llamado "sinovitis simétrica seronegativa remitente con edema con fóvea"17; este síndrome es de comienzo brusco, con sinovitis simétrica, que afecta a las vainas tendinosas de los flexores de los dedos, muñecas, manos y pies, con edema con fóvea de las manos y pies, factor reumatoide negativo y remisión con contracturas residuales en flexión de los dedos y las muñecas. Estos tres modelos, que en el anciano se consideran AR, nos confirman la heterogeneidad de este síndrome.
A veces es difícil distinguir la "AR benigna de la edad" de la PMR18. Las dos se caracterizan por marcada rigidez matutina de las cinturas escapular y pelviana, anemia y velocidad de sedimentación globular aumentada. La tumefacción de metacarpofalángicas, tobillos y codos, y la pérdida de movilidad pasiva de las muñecas, glenohumeral y caderas, apuntan a una artritis inflamatoria. Es importante distinguir la PMR de la AR a la hora de considerar el tratamiento inductor de remisión en la AR. Un fármaco como la hidroxicloroquina o sulfasalazina está indicado si el paciente no responde a dosis bajas de prednisona (menor de 10 mg al día), tiene sinovitis de las pequeñas articulaciones de las manos y pies, factor reumatoide positivo o signos de que la enfermedad va a seguir un curso deformante19.